动物繁育与功能基因组学研究组合作发现胚胎期低氧暴露引起卵巢颗粒细胞自噬性死亡
全球范围内,约有1.4亿人生活在海拔2500米以上的高海拔地区,其中8000万在亚洲。我国的高海拔人群主要分布在青藏高原。高海拔地区自然环境恶劣,其中低气压缺氧是高原环境的标志性特征之一。环境低氧和病理性缺氧会造成心脑血管功能异常和肺功能异常。生命发育早期,异常环境对生物体发育和代谢的影响尤为深远,即使环境因素的微小扰动也会对个体表型和健康状况产生持久影响。既往研究表明,低氧可损伤子宫或胎盘,引起肝脏和血管发育的表观遗传改变,影响胎儿发育。同时,急性子宫胎盘缺血-缺氧可引起发育中的脑组织氧化损伤。低氧暴露还会损伤雄性性腺发育和精子发生,但对胚胎期低氧暴露对雌性生殖和卵巢功能的影响尚缺乏系统研究。
中国科学院西北高原生物研究所和中国农业大学团队合作建立小鼠胚胎期低氧模型,发现胎儿期低氧暴露会造成雌性小鼠的卵巢卵泡发育异常从而导致生育力下降。通过培养原代颗粒细胞试验证实:胎儿缺氧导致卵巢颗粒细胞(Granulosa cells, GCs)线粒体功能障碍,并且导致GCs自噬性死亡。随后通过对不同处理小鼠的颗粒细胞就行转录组分析发现:胎儿缺氧造成的GCs自噬性死亡由PI3K/Akt/FoxO通路介导。此外,团队使用褪黑素处理胚胎期低氧小鼠的颗粒细胞,研究结果发现:褪黑素可改善低氧诱导的GCs自噬,并且缓解GCs的凋亡。为探究这一发现是否适用于人类,团队进一步使用褪黑素处理低氧培养的人源颗粒细胞系 (KGN细胞),发现褪黑素在KGN细胞中有同样的作用。最后,研究团队进行体内实验,褪黑素腹腔给药处理经历过胚胎期低氧的雌性小鼠,发现雌性小鼠生育能力及卵巢功能得到一定的恢复。以上结果表明,胚胎期低氧导致GCs过度自噬和线粒体损伤进而造成GCs死亡和增殖缺陷,导致卵巢功能和生殖能力下降。此外,褪黑素可以恢复GCs功能并改善卵巢功能衰竭的情况。本研究首次聚焦于胚胎期低氧对生殖的影响,并为提高低氧应激女性的生殖力提供了一个潜在的补救措施。
相关研究结果以 Fetal hypoxia expose caused autophagy in ovary granulosa cells via PI3K/Akt/FoxO1 pathway and mitigated by melatonin 为题,于11月11日在Journal of Advanced Research(Q1 ,IF=10.7)杂志以Article的形式在线发表。中国科学院西北高原生物研究所特别研究助理张璐瑶为论文第一作者,中国农业大学侯云鹏副教授为通讯作者。该工作得到了青海省科技重大专项“三江源区代表性动物基因资源保护与应用”,中国科学院青年创新促进会(2021432)和青海省“昆仑英才”项目等项目的资助与支持。
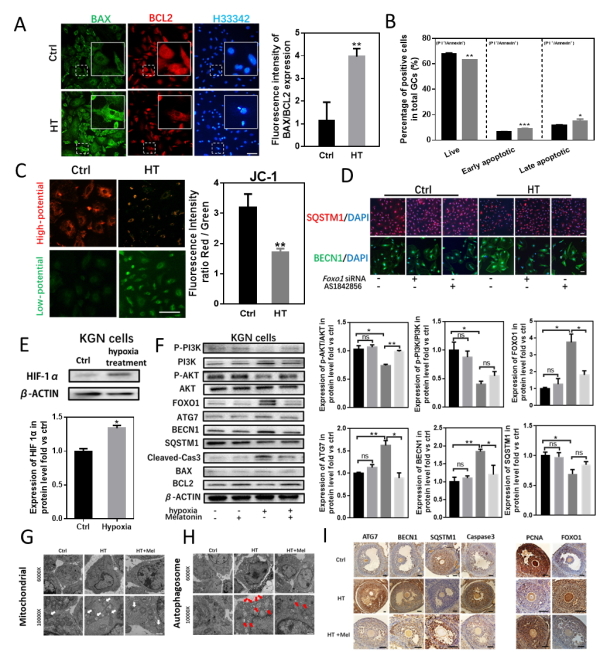
胚胎期低氧暴露通过PI3K/Akt/FoxO1通路引起卵巢颗粒细胞自噬性死亡
A:Bax/Bcl-2免疫荧光染色;B:流式分析凋亡细胞比例;C:JC-1染色指征线粒体膜电势;D: BECN1,SQSTM1免疫荧光染色指征细胞自噬水平;E:体外低氧条件培养KGN细胞;F:Western blot检测褪黑激素处理下对照组和胚胎期低氧 KGN细胞中PI3K、p-PI3K、AKT、p-AKT、Foxo1、Atg7、Becn1、SQSTM1、Lc3b、Bax/Bcl2、Cleaved-Cas3蛋白的表达;G-H: 对照和低氧小鼠颗粒细胞透射电子显微镜图像;I:用Atg7、Becn1、SQSTM1、Caspase3、Pcna 和Foxo1对从对照组,低氧组和褪黑素处理组卵巢中进行免疫组化染色

自噬通过Foxo1途径诱导胚胎期低氧雌性卵巢GCs死亡



 青公网安备 63010402000197号
青公网安备 63010402000197号